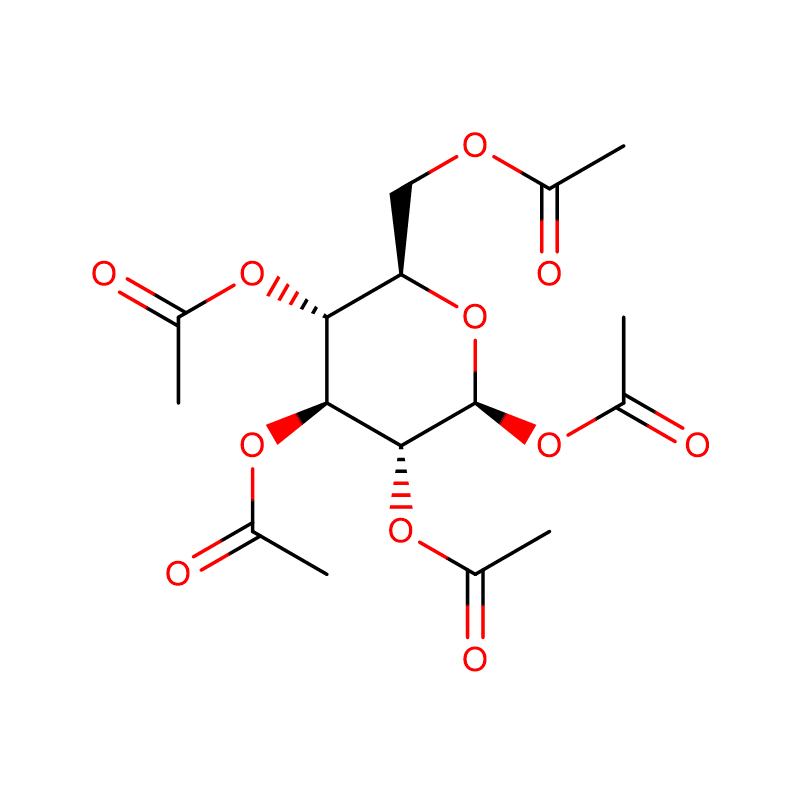
4-NITROFENIL-ALFA-D-MANOPIRANOSÍDEO CAS:10357-27-4 Pó esbranquiçado 98%
| Número de catálogo | XD90011 |
| Nome do Produto | 4-Nitrofenil-alfa-D-manopiranósido |
| CAS | 10357-27-4 |
| Fórmula molecular | C12H15NO8 |
| Peso molecular | 30301.25 |
| Detalhes de armazenamento | -2para -8°C |
| Código Tarifário Harmonizado | 29400000 |
Especificação do produto
| Água | <5% Karl Fische |
| Solubilidade | 1% em DMF é límpido e incolor |
| Pureza | 4-Nitrofenol grátis <200ppm |
| HPLC | >98% |
| Aparência | pó esbranquiçado |
Insights mecanísticos sobre uma família de alfa-manosidases dependente de Ca2+ em um simbionte intestinal humano.
Bactérias colônicas, exemplificadas por Bacteroides thetaiotaomicron, desempenham um papel fundamental na manutenção da saúde humana, aproveitando grandes famílias de hidrolases de glicosídeos (GHs) para explorar polissacarídeos dietéticos e glicanos hospedeiros como nutrientes.Essa expansão da família GH é exemplificada pelas glicosidases GH92 da família 23 codificadas pelo genoma de B. thetaiotaomicron.Aqui, mostramos que são alfa-manosidases que atuam por meio de um único mecanismo de deslocamento para utilizar os N-glicanos do hospedeiro.A estrutura tridimensional de duas manosidases GH92 define uma família de proteínas de dois domínios em que o centro catalítico está localizado na interface do domínio, fornecendo ácido (glutamato) e base (aspartato) assistência à hidrólise em um Ca(2+)- forma dependente.As estruturas tridimensionais dos GH92s em complexo com inibidores fornecem informações sobre a especificidade, mecanismo e itinerário conformacional da catálise.O Ca(2+) desempenha um papel catalítico chave ajudando a distorcer o manosídeo de sua conformação em cadeira de estado fundamental (4)C(1) em direção ao estado de transição.(Bibliografia: Nat.Chem.Biol.6, 125-32, (2010)
Cromatografia de afinidade frontal de glicoasparaginas de ovalbumina em coluna de concanavalina A-sepharose.Um estudo quantitativo da especificidade de ligação da lectina.
As interações da concanavalina A (ConA) imobilizada em Sepharose 4B com 10 glicoasparaginas derivadas da ovalbumina foram investigadas quantitativamente por cromatografia de afinidade frontal.Neste método, uma solução de carboidrato é aplicada continuamente a uma coluna de ConA-Sepharose e o retardo da frente de eluição é medido como um parâmetro da força da interação.A constante de dissociação (Kd) para cada sacarídeo com ConA pode ser determinada.Uma análise da ligação de p-nitrofenil-alfa,D-manosídeo mostrou que as propriedades de ligação de ConA não mudam essencialmente após imobilização em Sepharose 4B.Cada uma das glicoasparaginas de ovalbumina foi marcada com trítio pelo método de metilação redutora para análise.Uma comparação dos valores de Kd obtidos mostrou que a ligação de ConA varia consideravelmente com diferenças estruturais muito pequenas da cadeia de glicosil.Os resultados sugerem que ConA reconhece uma estrutura de cadeia glicosil específica, Man alfa 1-6(Man alfa 1-3)Man, na qual pelo menos um grupo hidroxila na posição C-3 da manose ligada a C-6 deve estar livre.